Гранулоциты — клетки, осуществляющие защитные функции в основном за счет фагоцитоза (нейтрофильные гранулоциты) и/или выполняющие внеклеточный цитолиз мишеней за счет секреции токсических субстанций, содержащихся в их гранулах (эозинофилы, базофилы, тучные клетки). Зрелые нейтрофилы характеризуются сегментированными ядрами и цитозольными гранулами. Все формы гранулоцитов происходят из общей полипотентной СК в костном мозге.
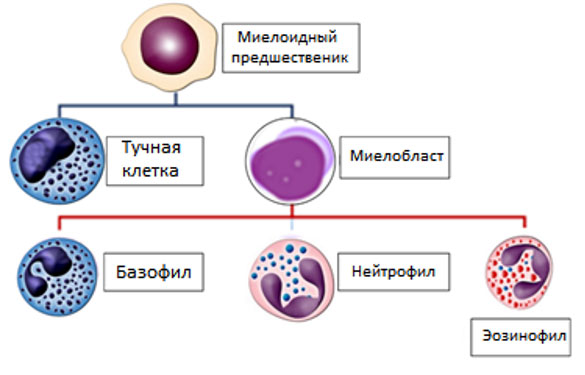
Нейтрофилы полиморфно – ядерные лейкоциты с сегментированным ядром и цитозольными гранулами. Классически считаются клетками, определяющими первую линию защиты врожденного иммунитета. Они быстро мигрируют в больших количествах к участкам воспаления, уничтожая патогены в первые дни заражения. Основной состав гноя. Уничтожения патогенов нейтрофилами происходит с помощью:
- фагоцитоза, способны поглощать микроорганизмы или частицы;
- дегрануляции, высвобождение набора белков из гранул (табл. 26), которые обладают антимикробными свойствами;
- NETоза, запрограммированная гибель нейтрофилов c высвобождением внеклеточных ловушек нейтрофилов (NET).
Состав гранул нейтрофилов

Нейтрофилы активно секретируют цитокины ИЛ-1β, ФНОα, ИЛ-6, ИЛ-12, ИЛ-17А, Г-КСФ и хотя отдельно по количеству генерируемых цитокинов нейтрофилы в десятки раз уступают другим лейкоцитам, но большое количество их в очаге воспаления приводит к тому, что цитокины нейтрофильного происхождения достигают значительных величин.
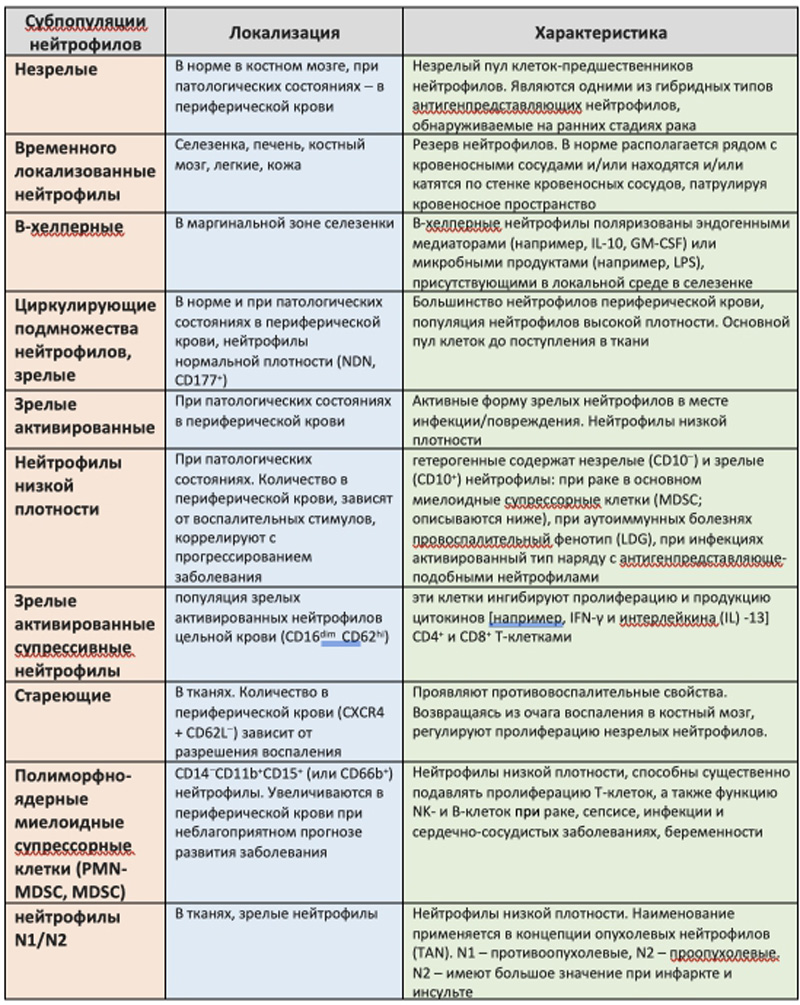
Морфологическая характеристика нейтрофилов определяется степенью зрелости клеток: юные, палочкоядерные и сегментоядерные нейтрофилы. Эти популяции можно дополнительно идентифицировать с помощью набора клеточных маркеров (незрелые нейтрофилы экспрессируют CD15 и CD11b, при достижения полной зрелости — CD16 и CD10. Сегментоядерные нейтрофилы — терминально дифференцированные клетки, которые во время воспаления могут мигрировать в ткани и выполнять свои эффекторные функции (например, фагоцитоз, производство реактивных форм кислорода (ROS) и уничтожение бактерий). Важно отметить, что нейтрофилы, могут быстро менять свои характеристики и поведение по мере того, как они активируются, стареют или входят в новую среду при остром или хроническом воспалении (реализуют совершенно разные эффекторные механизмы). При изучении множества параметров нейтрофилов (функции, маркеры клеточной поверхности, плавучесть, зрелость, локализация) были установлены некоторые фенотипы нейтрофилов (табл. 22).
Нейтрофильные гранулоциты обладают рядом свойств обусловливающих их участие в патогенезе острого воспаления это: богатый набор цитотоксических факторов; высокая чувствительность к всевозможным локальным изменениям гомеостаза; способность накапливаться в очагах поражения и инициировать цепную реакцию с выделением цитотоксических веществ и созданием локального перевеса в балансе эффектор-ингибитор; секреция биологически активных веществ, активирующих предшественников медиаторов воспаления.
Нейтрофилы принимают участие в реализации иммунокомплексного повреждения тканей и в антителозависимых цитотоксических реакциях.
Эозинофилы, базофилы, тучные клетки еще одна группа гранулоцитов. В отличии от нейтрофилов их защитная функция осуществляется не фагоцитозом, а мощной цитотоксической реакцией за счет дегрануляции.
Учитывая их полиморфизм, с клинической точки зрения следует различать клетки относимые к мукозальному иммунитету, которые заложены со времени эмбриогенеза (резидентные эозинофилы, тучные клетки) и традиционные эозинофилы и базофилы (продукты СККМ).
Тучные клетки богатые гранулами, иммунные клетки, которые распределены по всему организму в областях, где обычно возможно соприкосновение с микроорганизмами (барьерные ткани), таких как слизистые оболочки и кожа, а также в большинстве тканей, окружающих кровеносные сосуды и нервы. Традиционно выделяют две подгруппы тучных клеток: клетки соединительной ткани (CTMC) и клетки слизистой оболочки (MMC). По происхождению CTMC делят на самоподдерживающиеся, которые заселены в тканях до рождения, и СТМС, поддерживаемые костным мозгом.
Тучные клетки признаны регуляторными и эффекторными клетками как врожденного, так и адаптивного иммунитета, принимающими активное участие в развитии острых и хронических аллергических, аутоиммунных, воспалительных заболеваний и рака. Эти первичные, сигнальные клетки, связаны со многими иммунными и неиммунными клетками, которые реагируют на патогены и инициируют защитный ответ, высвобождая медиаторы, оказывающие различное действие на окружающие ткани (табл. 27). Они активно участвуют в формировании воспаления, аллергии и анафилаксии. Также тучные клетки играют важную роль в заживлении ран, ангиогенезе, иммунной толерантности, защите от патогенов и формировании гематоэнцефалического барьера.
Активация тучных клеток происходит за счет распознавания DAMP и/или PAMP и/или рецепторов, связанных с G-белком, так же активаторами могут служить белки комплемента.
Медиаторы тучных клеток и базофилов и их свойства
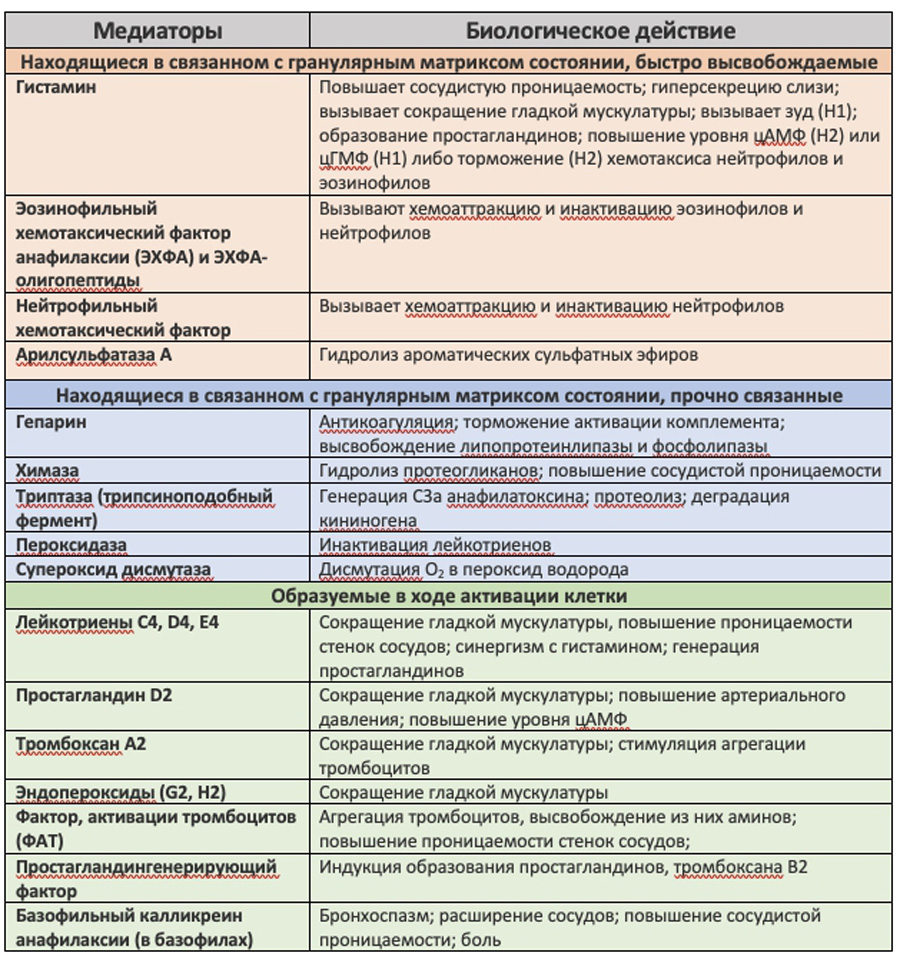
Отдельный механизм связан с рецептором IgE. Тучные клетки экспрессируют высокоаффинный рецептор (FcεRI) для Fc-области IgE. Этот рецептор имеет высокое сродство и необратимо связывается с IgE. В результате чего тучные клетки покрываются IgE. Как и любое АТ оно специфично к одному конкретному антигену (аллергену). Аллерген связывается с вариабельными участками IgE, находящимся на поверхности тучных клеток, активируют их с быстрым высвобождением (анафилактическая дегрануляция) содержимого гранул. Этим и обусловлены аллергические реакции.
Благодаря большому разнообразию других рецепторов, тучные клетки реагируют на различные типы стимулов, включая микробные, нервные, иммунные, гормональные, метаболические и химические триггеры. Именно взаимодействие тучных клеток и нервов способствует возникновению боли и зуда.
Базофилы наименее распространенный в периферической крови тип гранулоцитов, составляющий от 0,5 до 1% циркулирующих лейкоцитов. Морфологически, в отличии от других гранулоцитов крови, имеют базофильные гранулы, а в отличии от тучных клеток — сегментированное ядро, меньшие
размеры и округлую форму. Базофилы функционально тесно связаны с тучными клетками, хотя совершенно разные по своему происхождению и развиваются из разных гемопоэтических клонов. В отличие от тучных клеток, базофильные гранулы базофилов содержат меньше протеаз, кроме того, этих гранул в базофилах в целом меньше. Базофилы секретируют сравнительно немного активных веществ, однако по количеству выделяемого IL-4 они главный источник в организме, превосходя даже T-клетки.
На поверхности базофилов представлено большое число хемотаксических рецепторов, однако спектр Toll-подобных рецепторов (PRR) представлен скудно. Подобно тучным клеткам, базофилы имеют два типа рецепторов к иммуноглобулинам E: высокоаффинные (FcεRI) и низкоаффинные (FcεRII, или CD23), а также гистаминовые рецепторы H2. За счет этого базофилы быстро рекрутируются в лимфатические узлы, могут функционировать как антигенпрезентирующие клетки и имеют решающее значение для индукции дифференцировки Th2-клеток, а также связанных с ними воспалительных реакций после контакта с паразитами гельминтов или аллергенами. Все это дает основание предполагать, что базофилы в основном являются регуляторными, а не эффекторными клетками иммунитета.
Эозинофилы — разновидность гранулоцитов с крупными эозинофильными гранулами и сегментированным ядром. Это больше тканевые клетки, чем циркулирующие, поэтому в периферической крови их не более 150 клеток/мкл (1-3%). Дифференцировка эозинофилов регулируется цитокинами (IL-3, IL-5, GM-CSF). После созревания IL-5 контролирует миграцию эозинофилов из костного мозга в кровь.
Исходно эозинофилы локализуются в вилочковой железе, желудочно-кишечном тракте, матке и молочной железе. Эозинофилы способны секретировать на исходном уровне или при стимуляции большое количество разнообразных медиаторов (табл. 28).
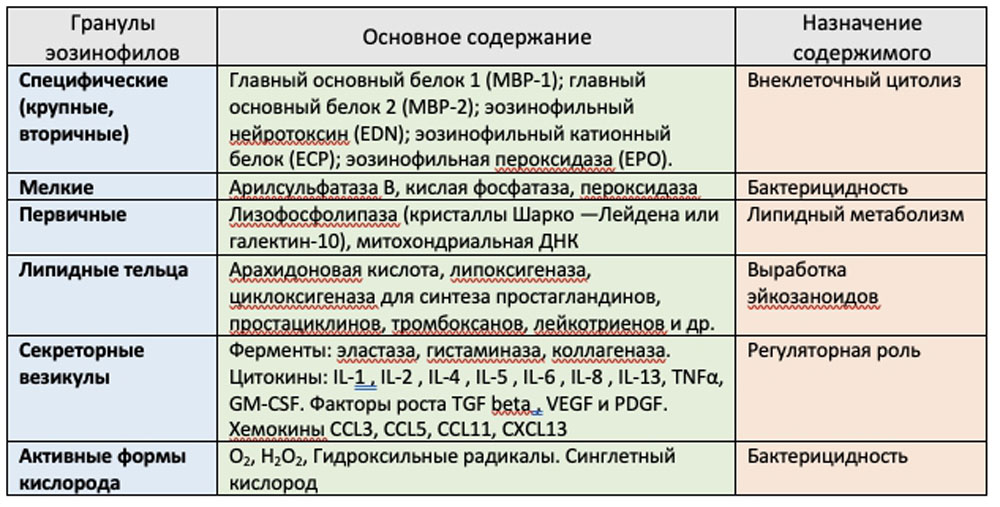
Состав гранул эозинофилов
Исходя из локализации (паренхима/барьерная ткань), морфологии ядра (кольцеобразная/сегментированная), поверхностному фенотипу, ответу на IL-5 различают два типа эозинофилов — резидентный (rEOS) и воспалительный (iEOS).
Характерной особенностью эозинофилов является их защитная антипаразитарная функция. Гельминты и их продукты их жизнедеятельности, медиаторы воспаления (прежде всего, гистамин) и хемокины, макрофагов, тучных и эпителиальных клеток привлекают эозинофилы в ткани. Оказавшись в месте повреждения, эозинофилы прикрепляются к поверхности паразитов за счет своего рецептора к С3b (большинство гельминтов активируют систему комплемента по альтернативному пути с образованием С3b), высвобождают свои цитотоксические гранулярные белки, а также предварительно сформированные цитокины и липидные медиаторы, способствуя уничтожению паразитов, развитию воспаления и повреждению тканей.
Эозинофилы являются эффекторами в метаболизме гистамина, секретируемого тучными клетками. Фермент гистаминаза, выделяемый эозинофилами, катализирует расщепление гистамина, так же эозинофилы фагоцитируют гистаминсодержащие гранулы тучных клеток, адсорбируют гистамин на своей плазмалемме, связывая его своими рецепторами, помимо этого эозинофилы секретируют фактор, тормозящий дегрануляцию и высвобождение гистамина из цитоплазмы тучных клеток.
Эозинофилы являются предполагаемыми антигенпрезентирующими клетками и играют существенную роль в активации тучных клеток, коммуникации и функции Т-клеток.